Hipra inicia l’assaig de la vacuna en adolescents amb la participació del Trueta
La farmacèutica està treballant per tancar contractes per entrar al mercat internacional abans que comenci la vacunació de la tardor
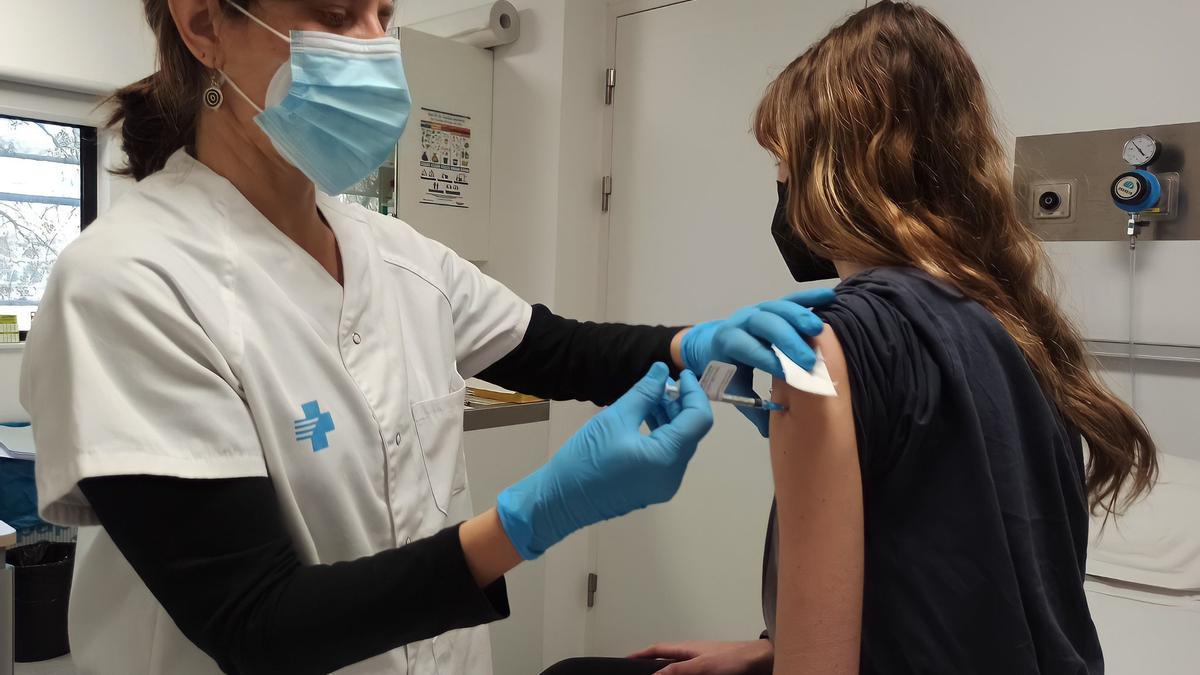
Una noia rep la vacuna d’Hipra en un dels assaigs. / ICS Girona
L’Agència Espanyola de Medicaments i Productes Sanitaris (AEMPS) ha autoritzat un assaig clínic de la vacuna contra la covid-19 de la farmacèutica biotecnològica Hipra per estudiar si la dosi de reforç és segura en adolescents entre dotze i disset anys que anteriorment han estat vacunats amb dues dosis de Comirnaty (Pfizer) i confirmar si aquesta dosi de reforç augmenta la resposta immunitària, és a dir les defenses, contra la covid-19. Per fer-ho, s’estudiarà si és ben tolerada i si és capaç de reactivar una resposta immunitària. S’avaluarà la seguretat a tots els participants, però la resposta immunitària només s’avaluarà en aquelles persones que no hagin passat prèviament el coronavirus.
A l’estudi, en què participaran 300 adolescents d’entre dotze i disset anys, comptarà amb cinc hospitals d’Espanya: Vall d’Hebron de Barcelona, Josep Trueta de Girona, HM Universitari Puerta del Sur de Madrid, HM Montepríncipe de Madrid i Hospital Universitari La Paz de Madrid. Aquests hospitals ja han començat el reclutament de persones voluntàries.
L’estudi comença una vegada la vacuna contra la covid-19, anomenada BIMERVAX®, ha estat aprovada per a la seva administració en adults, per l’Agència Europea del Medicament i per la Comissió Europea.
Pendents de la tardor
Un cop aprovada, el govern espanyol va ser el primer a confirmar la compra de 3,2 milions de dosis de la vacuna i fa un mes que ja es va fer efectiva. Segons fonts d’Hipra, la vacuna encara no s’ha començat a administrar a la població general, decisió que recau en una comissió de l’Agència Espanyola del Medicament. L’òrgan es reuneix mensualment i té sobre la taula determinar com i quan comença a administrar el vaccí i el conseqüent el repartiment entre les comunitats autònomes.
De forma paral·lela, Hipra està treballant per tancar més contractes per entrar al mercat internacional abans no comencin les campanyes de vacunació de tardor.
Cal recordar que la Comissió Europea va signar amb Hipra un contracte de compra de 250 milions de la vacuna. L’adquisició de vacunes es va fer de forma conjunta a escala europea. Un total de catorze estats hi tindran accés.
Finalment, per tal que la vacuna es pugui comercialitzar fora de la Unió Europea cal que l’Organització Mundial de la Salut també l’autoritzi.
- Salellas anuncia que Girona estudia "accions" contra els propietaris de pisos ocupats problemàtics que no actuïn
- Preparen una manifestació contra el turisme ciclista a Girona
- Girona aprova inicialment la zona de baixes emissions: restriccions viàries al centre de dilluns a divendres laborables
- El Girona fa tard amb Montilivi
- Els Mossos detenen, després d'una persecució, els autors d'un robatori a un camió a Vilademuls
- S'encén la façana d'un edifici de quatre plantes a Palafrugell
- Necrològiques , Noticies de Necrològiques - Diari de Girona
- Membres de la nova Associació Juvenil Marroquina del Ripollès: "Hi ha moltes ganes d'anar a votar el 12-M
